理化学研究所発の創薬スタートアップ企業。scFv抗体に細胞内の細胞質環境での凝集を防ぐペプチドタグ(Stabilizer peptide tag)を融合した分子を研究する。ウイルスベクターにSTAND配列をコードさせ投与する、またはSTAND配列をコードしたmRNAを脂質ナノ粒子で送達することで、標的細胞内で安定性scFv発現させるベクター化抗体のアプローチを取る。2022年にラクオリア創薬との提携を発表し、特定のイオンチャネルを標的とする細胞内抗体の共同研究を行い、出資も受けている。CEOの樺山博之先生(理化学研究所)が2020年に論文を報告しており、scFvやVHH抗体の生体内での等電点(pI。分子が帯びる電荷が中性になるpH)に着目。低いpH環境(pH6.6)で抗体の安定化が促進されるように、高い負電荷と低い等電点を持つペプチドタグを抗体に融合している。
Minato-ku, Tokyo, Japan
この企業の詳細情報の作成をご希望の方は、お気軽にリクエストください
設立 2019 年 | 推定従業員数 1-10 名 | 累計調達額 $0M Ave:155.4M Med:22.5M | 提携企業数 1件 Ave:3.3 Med:1 | 論文数 0件 Ave: 13.2 Med: 4 | 特許数 1件 Ave: 13.2 Med: 4 |
テクノロジー
STAND Technology
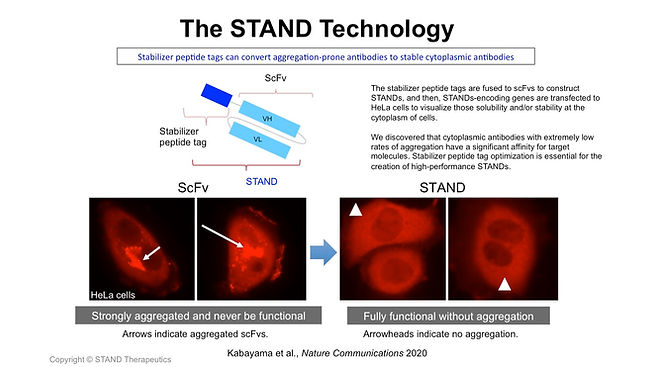
scFv抗体やVHH抗体に、細胞内の細胞質環境での凝集を防ぎ安定性を高めるペプチドタグ(Stabilizer peptide tag)を融合した分子。
CEOの樺山博之先生(理化学研究所)が2020年に論文を報告しており、高い負電荷と低い等電点を持つペプチドタグをscFv抗体に融合している。
scFvは細胞質で発現させると、誤った折りたたみや凝集を起こす傾向があり課題となっていた。細胞質pHは6.3〜7.5の範囲で変化するため、低pH環境に予期せず暴露されることに対して、ペプチドタグを融合することでpH 6.6であっても正味の負電荷が強い細胞質抗体を(配列置換などを行わずに)構築できる。
論文ではAAVベクターにSTAND抗体をコードし、マウス脳への局所投与によって凝集を起こさず細胞質に抗体が発現することを確認(Fig.4,5)。
Syt I/II-C2Aに結合するscFvのペプチドタグ融合分子(scFv-A36)をコードするAAVベクターのマウス脳への投与で、ドーパミン作動性ニューロンのSyt I阻害活性を確認している(Fig.7)。
パイプライン
パイプライン名 | 開発フェーズ | 対象疾患 | 標的分子/作用機序 | モダリティ | パートナー企業 |
|---|---|---|---|---|---|
None | 探索 非臨床 P1 P2 P3 申請 上市 |
提携企業
提携企業 | 日付 | プレスリリース |
|---|---|---|
RaQualia Pharma | 2022-08-15 |

