Bi-specific抗体を用いて、標的タンパク質分解創薬を行う企業。片方のアームが膜タンパク質や細胞外タンパク質などの標的タンパク質に結合し、もう片方のdegrader binding armは、E3 ligaseや細胞内への取り込みを行う受容体(internalizing receptorやchemokine/cytokine receptor)に結合し、ユビキチン-プロテアソーム系やリソソームによるタンパク質分解を誘導する。degrader binding armは抗体やサイトカインが用いられて、3種類のプラットフォーム(AbTac, TrainTAC, KineTAC)に分かれる。抗体を用いる技術は、E3 ligaseに結合するAbTacと、internalizing receptorに結合するTrainTACがある。サイトカインを用いる技術、サイトカイン受容体ターゲティングキメラ(KineTAC)は、CXCL12を用いてサイトカイン受容体のCXCR7に結合し、サイトカイン媒介性のInternalizationを起こし、もう片方のアームに結合した標的タンパク質とともにLysosomeに移行し分解が起こる仕組み。CXCR7以外のサイトカイン受容体を活用することも可能で、IL-2を用いてIL-2受容体をターゲティングするKineTACなどを報告。これまでに、PD-L1やHER2、EGFRの分解を確認したデータを報告している。
San Mateo, California, United States
この企業の詳細情報の作成をご希望の方は、お気軽にリクエストください
設立 2022 年 | 推定従業員数 11-50 名 | 累計調達額 $203.1M Ave:162.1M Med:21.2M | 提携企業数 1件 Ave:3.6 Med:1 | 論文数 3件 Ave: 12.4 Med: 3 | 特許数 2件 Ave: 17 Med: 4 |
テクノロジー
EpiTAC
組織特異的に細胞外の標的タンパク質を分解するbi-specific抗体。
抗体の片方のアームはtarget binding armで、標的である膜タンパク質や細胞外タンパク質に結合する。
もう片方のdegrader binding armは、膜貫通E3 ligaseや細胞内への取り込みを行う受容体(internalizing receptorやchemokine/cytokine receptor)に結合し、ユビキチン-プロテアソーム系やリソソームによるタンパク質分解を誘導する。degrader binding armには、抗体やサイトカインが用いられ、用いる分子によって3種類のプラットフォーム(AbTAC, TrainTAC, KineTAC)に分かれている。
AbTAC
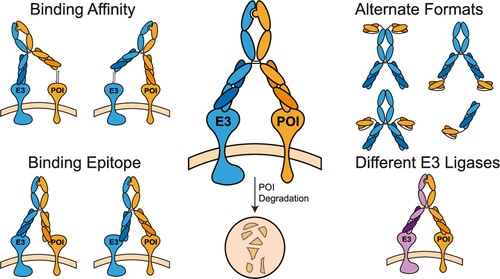
抗体が標的タンパク質と膜貫通E3 ligaseに結合して、ユビキチン-プロテアソーム系によるタンパク質分解を誘導する技術。
2022年に発表された論文によると、分解標的としてPD-L1やEGFR、degraderとしてRNF43やZNRF3 E3 ligaseを使用している。
この論文ではIn vitroやIn vivoの概念実証の他、degraderと標的の発現量と分解効率の関係や、RNF43とZNRF3に関連するWntシグナルがAbTAC投与時には活性化されないことを示す実験を行っている。
KineTAC
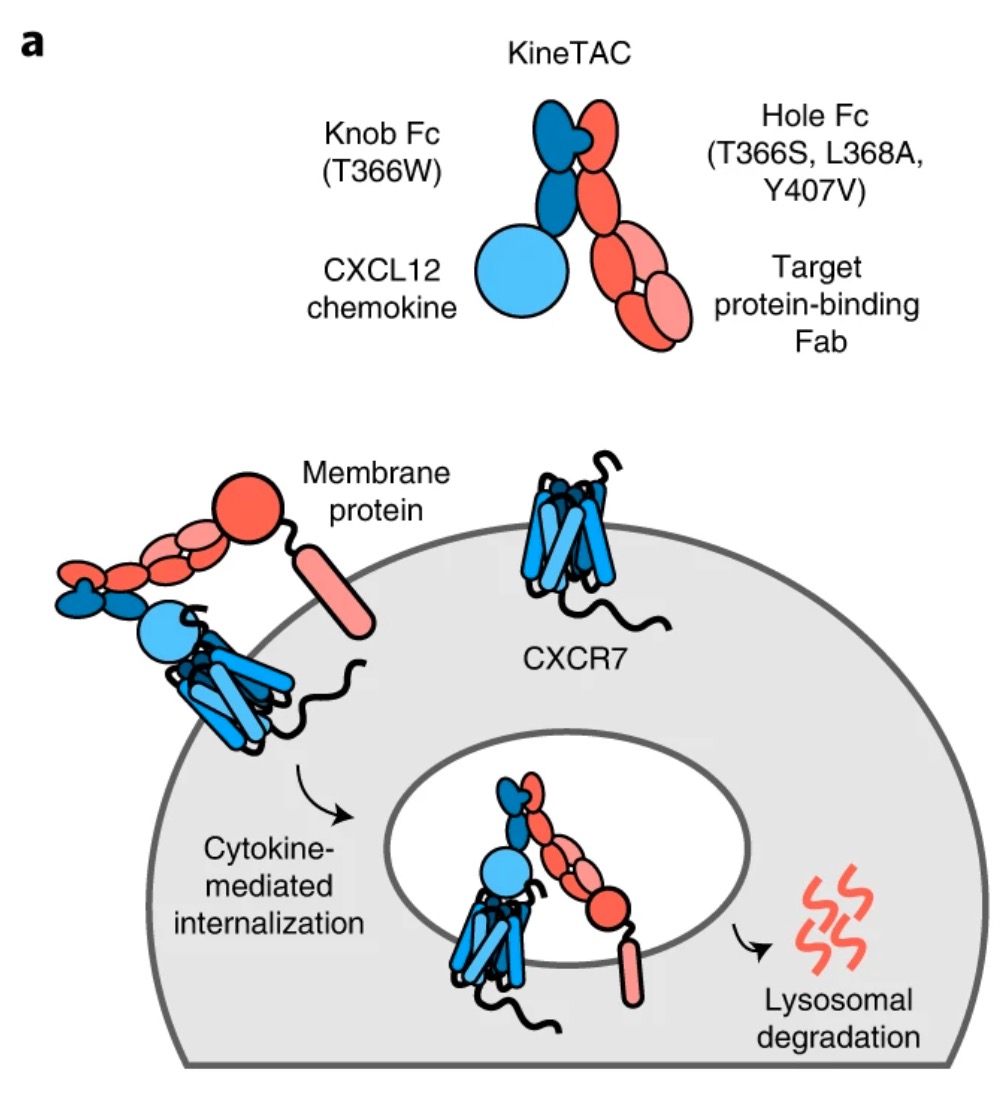
抗体が標的タンパク質と結合した状態でサイトカイン受容体媒介性のInternalizationを引き起こし、標的タンパク質をリソソームに移行させ分解する技術。
2022年の論文で技術が紹介されている。
PD-1とCTLA4のbi-specific抗体が、PD-1の阻害だけでなく分解を引き起こすことから着想を得ており、CytokineやChemokineドメインを片方のアームに持つ(サイトカイン受容体に結合する)bi-specific抗体を作成。
論文では、CXCR7ターゲティングのためにCXCL12ドメインやCXCL11ドメイン、vMIPIIドメインなどを比較して、CXCL12ドメインが効率的にCXCR7に結合しInternalizaitonを誘導することを確認している。
TrainTAC
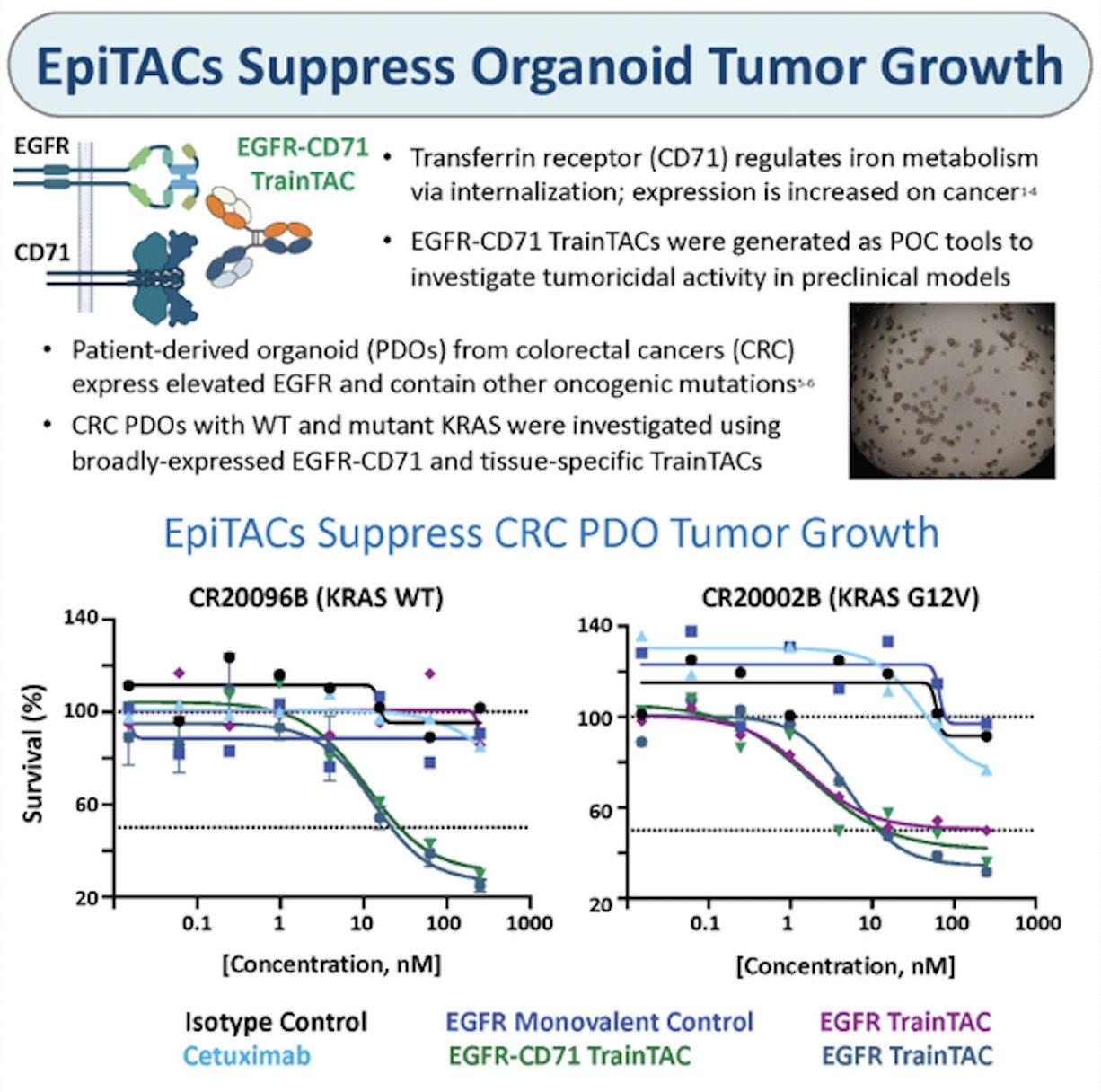
抗体が標的タンパク質とinternalizing receptorに結合し、リソソームによるタンパク質分解を誘導する技術。
AACR2024における会社発表資料で、EGFRを分解標的とするTrainTACを使ったIn vitro及びIn vivo実験について説明鎖れている。
TrainTACのdegraderとしては、トランスフェリン受容体のCD71が用いられている。
In vitro試験ではウェスタンブロットなどを用いて、TrainTACによりEGFRが膜から除去されたことを示すデータや、EGFRのシグナルが阻害されることを示している(Fig.3-6)。
また、大腸がん患者由来腫瘍組織を用いたオルガノイドで細胞傷害活性を確認(Fig.7)
In vivo実験では、NSCLCのXenograftモデルを用いて、Osimertinibと比較して生存期間が延長するデータを示しており、EGFR変異(L858R/T790M)の薬剤耐性に有効であることを示している(Fig.11)。
AACR2025では、cMETのdegraderとして働くTrainTAC分子をポスター事例として報告している。片方のarmがcMETに、もう片方のarmがトランスフェリン受容体のCD71に結合し、分解を誘導する。また、CD71以外の受容体についても探索を行い、腫瘍細胞でcMETと共に発現が増加している受容体を結合標的として特定(Fig.5)。CD71と比較して、担がんマウスモデルにおいてより強力な抗腫瘍活性を示すことを確認している(Fig.8)。
加えて、このTrainTAC分子をADC化する研究にも取り組んでいる(Fig.9-10)。Internalizationを誘導する作用機序のため、細胞内に抗体が取り込まれる効率は高く、TrainTACの作用機序とマッチする戦略と言える。
EpiAtlas
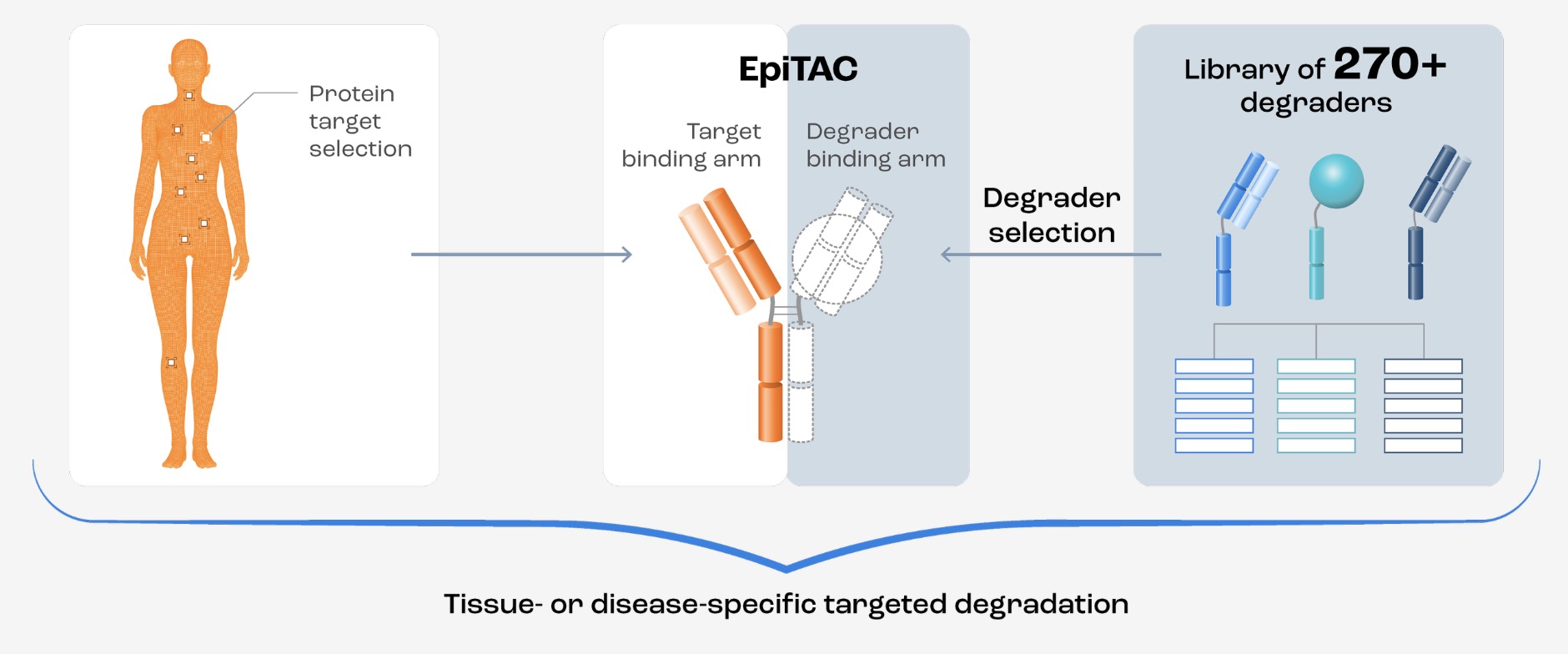
270種類以上のdegrader binding armのライブラリ。
AACR2024のポスター事例では、腫瘍組織に高発現するdegraderを遺伝子発現情報に基づいて選択し(Fig. 2)、候補degrader群を用いてEGFRの分解を行い、分解されたかどうかをEGFR抗体を用いたflow cytometryによって検証することで、活性の高いdegraderを特定している(Fig.3)。
パイプライン名 | 開発フェーズ | 対象疾患 | 標的分子/作用機序 | モダリティ | パートナー企業 |
|---|---|---|---|---|---|
EPI-326 | 探索 非臨床 P1 P2 P3 申請 上市 | Non-Small Cell Lung Cancer (NSCLC) | EGFR degrader bi-specific Ab | 抗体医薬 | |
Undisclosed | 探索 非臨床 P1 P2 P3 申請 上市 | Cancer | bispecific antibody EpiTACs | 抗体医薬 | |
Undisclosed | 探索 非臨床 P1 P2 P3 申請 上市 | Cancer | bispecific antibody EpiTACs | 抗体医薬 | |
Undisclosed | 探索 非臨床 P1 P2 P3 申請 上市 | Immunological disorders | bispecific antibody EpiTACs | 抗体医薬 | |
Undisclosed | 探索 非臨床 P1 P2 P3 申請 上市 | Immunological disorders | bispecific antibody EpiTACs | 抗体医薬 |
EpiBiologics と似ている企業
ペプチド抗原を修飾リポソーム粒子に封入して投与するワクチン、および神経変性疾患のタンパク質凝集体に結合する中枢移行性の低分子化合物を開発する企業。修飾リポソーム技術(SupraAntigen)は、リポソーム表面にアジュバント分子の提示、並びにパルミチン鎖アンカーに連結したAβペプチドなどの標的抗原ペプチドをB-cell peptideとしてリポソーム表面に提示し、リポソーム内に免疫刺激用のT cell peptideを含めることで、標的抗原に対する抗体産生を効率的に誘導する特徴がある。ワクチンとしての利用以外に、動物免疫による抗体作成用の抗原として利用することもできる。タンパク質凝集体に結合する中枢移行性の低分子化合物の探索では、皮質ニューロンの細胞アッセイによって化合物のスクリーニングを行い、Tauやα-synucleinに結合する化合物を特定。共にPETトレーサーとして研究開発を行っている。これまでにp-Tau抗体の品目SemorinemabでGenentechと提携、pTauワクチンでJanssenと提携、Tau PETトレーサーでEli Lillyと提携し、大手製薬企業との提携実績が豊富である。

