CAR-T療法やγδCAR-T、CAR-NK療法を開発する中国の創薬ベンチャー。BCMAを標的とするCAR-T療法の品目(Carvykti/Ciltacabtagene Autoleucel)がJanssen Pharmaと提携しFDA承認を取得している。抗体スクリーニングを自社で行い、BCMA以外にCD19, CD20, CD22, CD70, GPRC5D, DLL3, Claudin18.2, Guanylyl cyclase-C (GCC)を標的とした品目を血液癌、固形がん、自己免疫疾患を対象に開発する。自己免疫疾患を対象に開発されている自家CAR-Tの品目は、CD19, CD20, CD22の3種類の抗原を認識する。製造拠点を米国、欧州、中国に保有しグローバルな供給体制を確立。SCLCを対象とするDLL3標的CAR-Tの品目は腫瘍微小環境の免疫抑制シグナルを回避する工夫を施しており、Novartis社に導出を行っている。
Piscataway, New Jersey, United States
この企業の詳細情報の作成をご希望の方は、お気軽にリクエストください
設立 2014 年 | 推定従業員数 1001-5000 名 | 累計調達額 $750.5M Ave:162M Med:21.2M | 提携企業数 6件 Ave:3.6 Med:1 | 論文数 67件 Ave: 12.4 Med: 3 | 特許数 133件 Ave: 17 Med: 4 |
テクノロジー
Global Manufacturing Sites

2024年の企業紹介プレゼン資料にて、グローバルな開発、供給を製造キャパシティとして、米国、欧州、中国の3テリトリーで製造拠点を自社で保有している強みを紹介している(p.10)。上市品として自家BCMA CAR-T製品(CARVYKTI)を持つため商業生産の経験があり、現在commercial製造は米国で実施しており、現在欧州(ベルギー)、及び中国でのcommercial製造の準備を進めている。
グローバルでの自社製造による開発体制を整えていることがユニークな強みだと感じる。
また、2025年11月の企業プレゼンテーションにて、上市品のCARVYKTIの商業化・プロモーションにおいてJohnson & Johnson (Jansssen)との提携を行っており(p.6)、結果として他社CAR-T製品と比較してローンチ後の世界売上の立ち上がりが一番に早い実績を紹介(p.10)。
グローバルでの商業生産のスケールアップ、実績を積んでいる状況が伺える。
CARVYKTIの治療を米国で受けられる医療機関の数も増加しており、2025年11月の企業プレゼンテーションにて、CARVYKTIの治療に対応する医療機関は2022年の44サイトから2025年に131サイトに拡大し、2026年には地域のcommunity/regional hospitalでも治療を受けられるようにしていく予定だと紹介している(p.12)。
Novartis社に導出した自家DLL-3 CAT-Tの品目について、Novartis社が保有する製造技術T-Charge技術をLegend社に提供することがプレゼン資料(p.12)、およびプレスリリースで紹介されている。Ex vivoでのT細胞増殖期間を短くし、患者投与後に体内でT細胞増殖を起こす技術で、製造期間(投与までのラグ)を短縮する。今後T-Charge技術がLegend社の他の品目にも適用されるようになるかどうかは不明だが、上市済みCAR-T品目を持つNovartis社との提携によってLegend社の製造面での経験が強化されていくと思われる。
また、2022年のR&D Dayプレゼン資料にて、他家γδCAR-Tの製造プロセスについて閉鎖系・semi-automatedなプロセスを構築済みで、1 leukopakから1,000 dose分の調製を行っていると説明している(p.83)。
製造プロセス関連技術について詳細は開示されていない。γδCAR-T細胞のExpansion効率や、製造した細胞はTcm細胞(CD62L+CD45RA-)の割合が多いこと、T cell exhaustion markerのPD-1・TIGITの発現が低いデータを紹介している(p.84)。
Novartis社のT-Charge技術については、2023年にNovartis社から論文が報告されている。Legend社のCAR-T品目ではなく、Novartis社のYTB323の品目を製造。文献上では、一番のポイントは培養期間を短縮したことにあるとしている(細かい工夫を非開示としている可能性もある)。
従来9-10日間かかっていた、製造サイトでのCell enrichment 〜 Formulationまでのプロセスを、培養時間を24時間以内に短縮し、合計2日間の工程でFormulationまでのプロセスを行っている(Fig.1)。
結果として、Ex vivoで長期培養を行ったときよりもTscm細胞割合(CD45RO–/CCR7+ Tcells)が高く保たれることを、フローサイトメトリーによる分析(Fig.2A, B)、およびシングルセルシーケンスによる分析で確認している(Fig.2C)。
VHH sdAb, Multispecific CAR
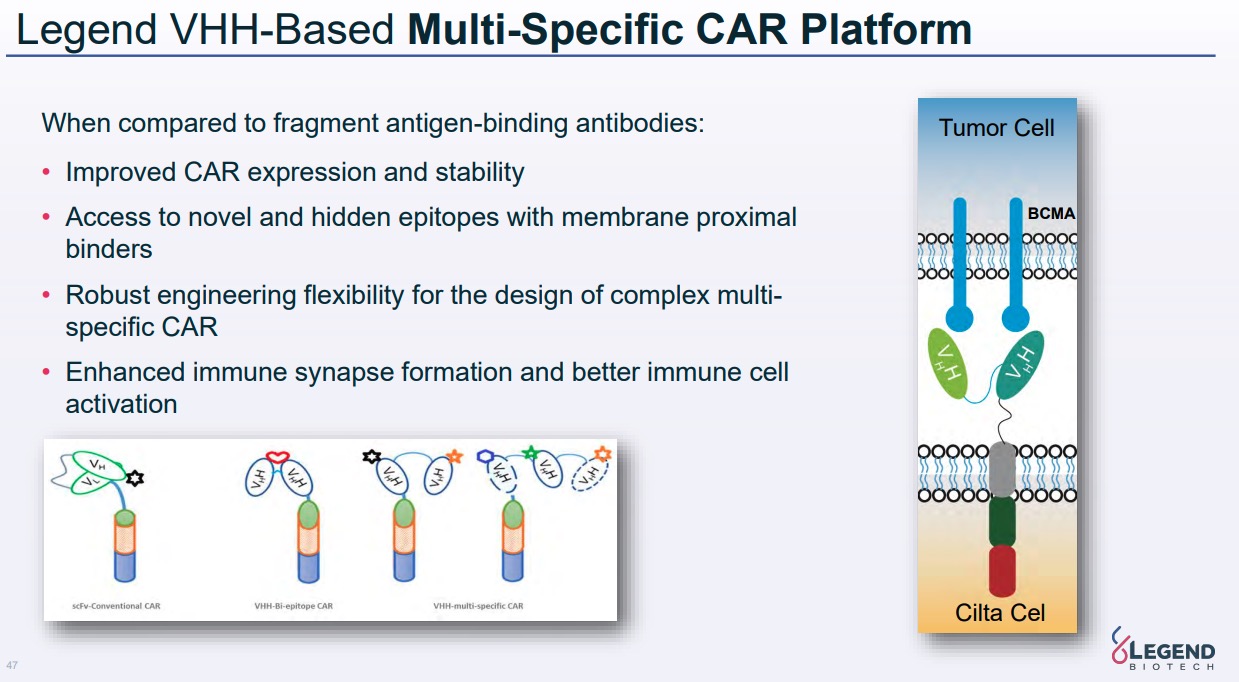
CAR遺伝子の細胞外ドメインは、scFvを用いた品目も保有するが(例:GPC3 CAR-TのLB2101)、主にはシングルドメイン抗体のVHHを使用している。
2022年のR&D Dayプレゼン資料にて、単一のVHHドメインを提示するCLDN18.2 CAR-T (LB1908, p.57)やGCC CAR-T (LCAR-G08T, p.65)の他に、タンデムにVHHドメインを提示し単一の抗原を認識するDLL-3 CAR-T(LB2102, p.60)などの品目が紹介されている。
VHHドメインをタンデムに連結することでMulti-specificityを実現する戦略を取っており、DLL-3 CAR-Tの例のように同一タンパク質の2種類の異なるエピトープをタンデムVHHによって認識するアプローチ(VHH-Bi-epitope CAR)や、タンデムVHHの各VHHがそれぞれ異なる抗原を認識するbi-specific, tri-specificのアプローチについて研究を行っていることが分かる(p.47)。
VHH抗体のスクリーニング手法については、ハイスループットなスクリーニングを実施していると記載があるが(p.46)詳細は開示されておらず、一般的なphage displayなどを用いているのかどうかは不明。
パイプライン表にNHL/ALLを対象にPhase 1段階にあるCD19, CD20, CD22を標的とするMulti-specific CAR-Tの品目の記載があり(p.55)、2022年に特許を申請している。CD19, CD20, CD22それぞれの抗原に結合するVHH抗体をタンデムに連結したCAR遺伝子を使用していることが伺える(5.Detailed Description参照)。2025年時点で本品目はパイプライン表になく、適応疾患を変更し自己免疫疾患を対象に開発されている。
また、単一のCAR遺伝子にタンデムなVHHドメインを提示するだけでなく、2種類のCAR遺伝子にそれぞれ単一のVHHドメインを提示するDual CAR-Tについても研究を行っている(p.52)。片方のCAR分子は活性化シグナルによってCAR-T細胞を活性化させ、もう片方のCAR分子はサイトカインを発現するArmored機能を担うように設計されている。
サイトカイン発現Armored γδCAR-Tにおいてサイトカイン分泌、細胞増殖が見られるデータが示されている。
Armored CAR-T
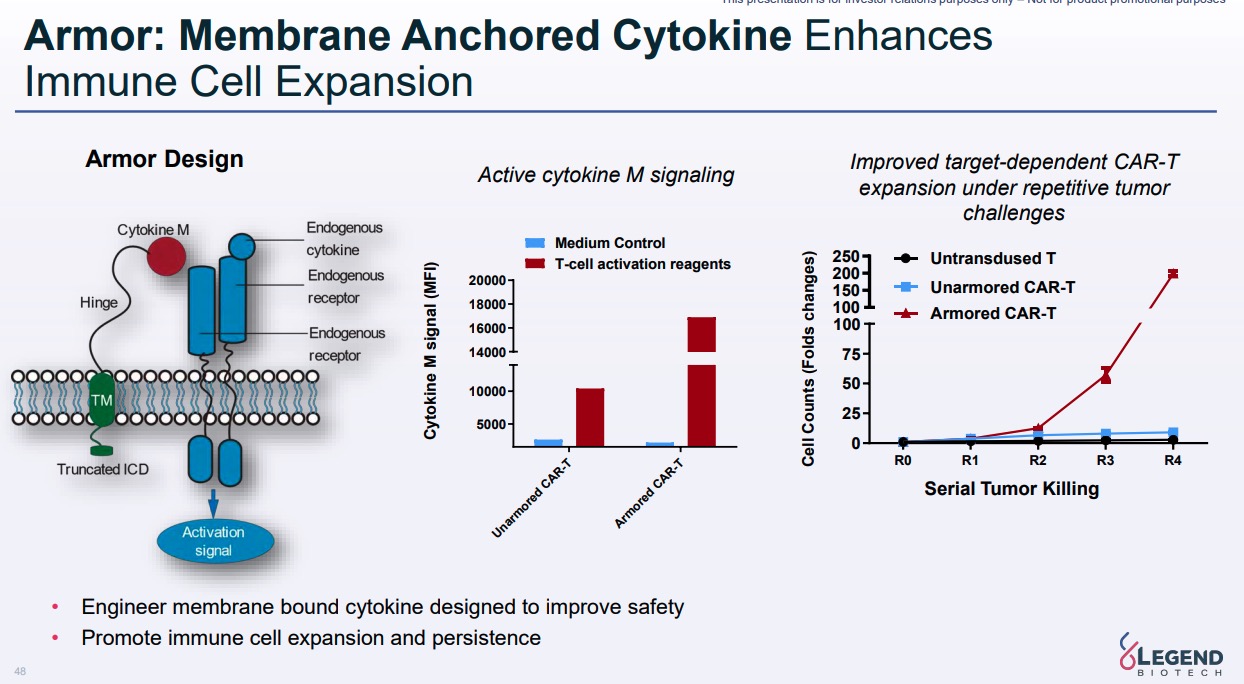
サイトカイン発現については、分泌型のサイトカインを発現させる以外のArmored CAR-Tアプローチについても紹介されている。膜にアンカーされたサイトカイン分子を発現させた例では、サイトカイン名は開示されていないが、サイトカイン分子が膜表面に固定されているため、CAR-T細胞の内在性サイトカイン受容体がクラスター化して活性化する反応を安定的にサポートする仕組みで作用する(p.48)。
腫瘍細胞と複数ラウンド反応させる試験でArmored CAR-Tの細胞増殖が起こることを示している。
また、分泌型のサイトカインをコードして発現させるが、サイトカイン分泌を阻害する仕組みを細胞に持たせることで細胞内のサイトカイン濃度を高め、同時にパラクリン的に周囲の細胞を活性化させないことで安全性を高めることを狙ったArmored CAR-Tが紹介されている(p.49)。
また、腫瘍微小環境における免疫抑制シグナルを回避する、もしくは免疫活性化シグナルに変換する受容体(Switch Receptor)を発現させたArmored CAR-Tが紹介されている(p.50, 51)。
GPC3 CAR-TのLB2101の品目では免疫抑制シグナルを活性化シグナルに変換するSwitch Receptorを発現させており(p.59)、DLL-3 CAR-TのLB2102の品目では免疫抑制シグナルを回避する受容体を発現させている(p.60)。
2021年の特許では、PD-L1/CD28キメラスイッチ受容体、およびTGF-βRIIの細胞内ドメイン切断型であるドミナントネガティブ変異体について言及されており、このどちらかを使用していると考えられる。
また、CRISPR screenによってCAR-T細胞の任意の因子をノックアウトし、プールしたCAR-T細胞の活性を評価することで、CAR-T細胞の効果を増強する新規のノックアウト遺伝子を特定していることを紹介している(p.53)。対象の遺伝子名は開示されていない。
Non-gene editing Universal CAR-T
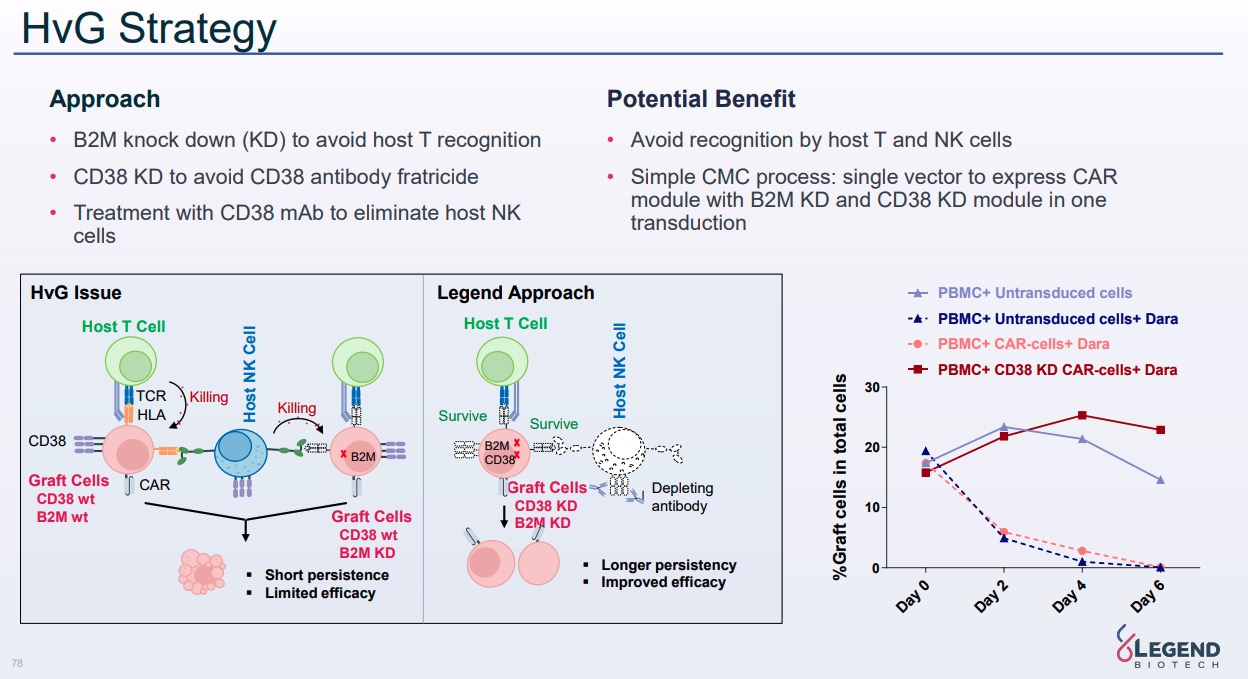
遺伝子編集を行わずに他家のCAR-T, CAR-NK細胞を構築する技術。CAR-NKの項目で紹介されている技術のためCAR-Tについても同様の技術を用いてるかどうかは不明だが、
1.B2MとCD38を(ノックアウトではなく)ノックダウンする
2.宿主のNK細胞をCD38抗体の投与によって除外する
アプローチを取っている(p.78)。CAR遺伝子をコードする単一コンストラクトにB2MとCD38のノックダウンを行う因子も一緒にコードされており、製造面手の複雑性を回避しているとのこと。
また2022年の特許では、腫瘍抗原に対するCARに加えて免疫細胞抗原であるCD8, CD30, CD33, CD70などの分子に対するCAR遺伝子を追加で発現させる、もしくは組み換えTCR複合体を発現させるCAR-Tについて言及されており、腫瘍細胞だけでなく宿主の免疫細胞に対しても作用することで他家細胞であるCAR-Tを定着させる研究を行っている可能性がある。
In vivo CAR-T
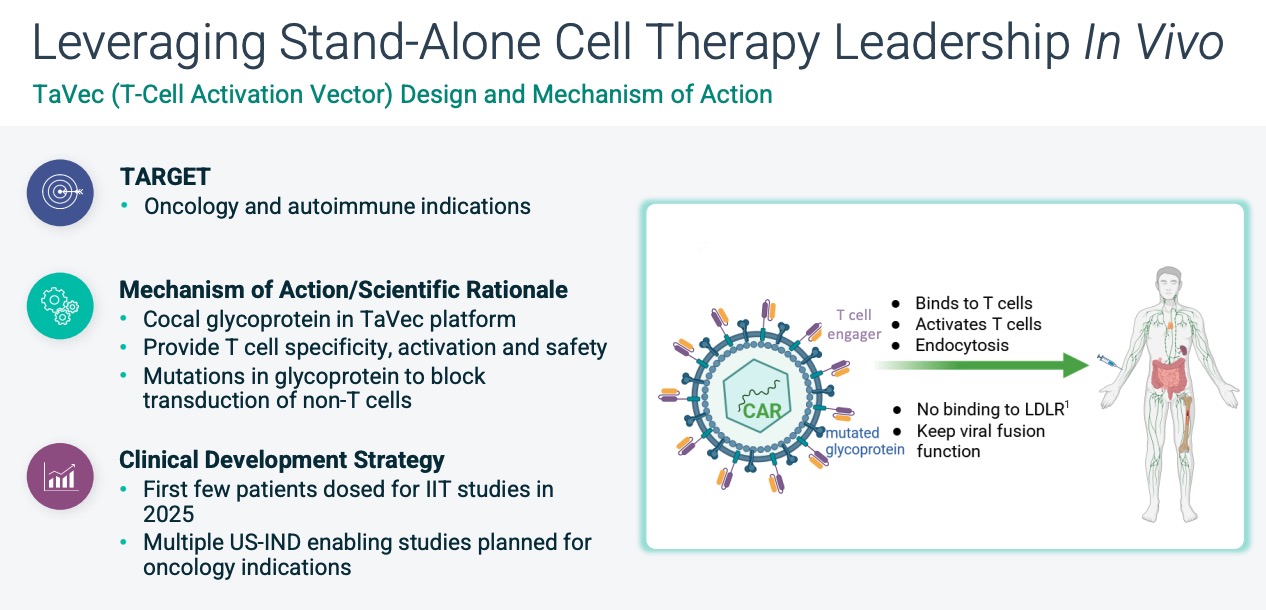
2025年11月の企業プレゼンテーション資料にて、In vivo CAR-Tの研究に取り組んでいることを紹介している(p.22)。
TeVec (T-cell Activation Vector)と呼ばれるベクターを使用してT細胞にCAR遺伝子を導入する技術が図示されており、図と説明文から、レンチウイルスベクターにT細胞ターゲティングscFv分子を提示し、かつ変異糖タンパク質を用いることで非T細胞への導入を防ぎ、T細胞への形質導入の特異性を高めている技術だと思われる。
2025年に特許が申請されており、低密度リポタンパク質受容体(LDL-R)への結合性が低下したウイルス糖タンパク質変異体を使用している。
野生型VSV-Gエンベロープではなく、野生型コカルウイルス糖タンパク質(COV-G)由来の配列、もしくはVSV-G変異体、MARAV-G変異体を使用しており(項目[0008-0011])、LDL-Rへの結合が弱まることで、LDL-Rを発現する様々な細胞(非T細胞)へのオフターゲット感染が減少する仕組み。
様々な変異体エンベロープを構築し(Table 1-3)、CD3 scFvを提示したレンチウイルスベクターを構築しており、Jurkat細胞とヒトPBMCへの感染を評価してT細胞特異性を推定している(Fig.16, Table 6)
パイプライン名 | 開発フェーズ | 対象疾患 | 標的分子/作用機序 | モダリティ | パートナー企業 |
|---|---|---|---|---|---|
CARVYKTI | 探索 非臨床 P1 P2 P3 申請 上市 | Multiple Myeloma (MM) | BCMA, Autologous CAR-T cell therapy | 細胞治療 | Johnson & Johnson |
Autoimmune (CD19×CD20×CD22) | 探索 非臨床 P1 P2 P3 申請 上市 | Autoimmune disorders | CD19, CD20, CD22, Autologous CAR-T cell therapy | 細胞治療 | |
Colorectal (GCC) | 探索 非臨床 P1 P2 P3 申請 上市 | ColoRectal Cancer (CRC) | GCC, Autologous CAR-T cell therapy | 細胞治療 | |
Gastric & Pancreatic (Claudin 18.2) | 探索 非臨床 P1 P2 P3 申請 上市 | Gastric Cancer,Pancreatic Cancer | Claudin 18.2, Autologous CAR-T cell therapy | 細胞治療 | |
MM (CD19×GPRC5D) | 探索 非臨床 P1 P2 P3 申請 上市 | Multiple Myeloma (MM) | CD19, GPRC5D, Autologous CAR-T cell therapy | 細胞治療 | |
SCLC & LCNEC (DLL3) | 探索 非臨床 P1 P2 P3 申請 上市 | Small Cell Lung Cancer (SCLC),Large Cell Neuroendocrine Carcinoma (LCNEC) | DLL3, Autologous CAR-T cell therapy | 細胞治療 | Novartis |
Autoimmune (CD19×BCMA) (CD19×CD70) | 探索 非臨床 P1 P2 P3 申請 上市 | Autoimmune disorders | CD19×BCMA, CD19×CD70, CAR-T cell therapy | 細胞治療 | |
MM (BCMA) CAR-NK | 探索 非臨床 P1 P2 P3 申請 上市 | Multiple Myeloma (MM) | BCMA, Allogeneic CAR-NK cell therapy | 細胞治療 | |
NHL (CD20) CAR-αβT | 探索 非臨床 P1 P2 P3 申請 上市 | Non-Hodgkin’s Lymphoma (NHL) | CD20, Allogeneic CAR-αβT cell therapy | 細胞治療 | |
NHL (CD19×CD20) CAR-γδT | 探索 非臨床 P1 P2 P3 申請 上市 | Non-Hodgkin’s Lymphoma (NHL) | CD19×CD20, Allogeneic CAR-γδT cell therapy | 細胞治療 | |
NHL (CD19×CD20) | 探索 非臨床 P1 P2 P3 申請 上市 | Non-Hodgkin’s Lymphoma (NHL) | CD19×CD20, in vivo CAR-T cell therapy | 遺伝子治療 |
提携企業
提携企業 | 日付 | プレスリリース |
|---|---|---|
Janssen Pharma | 2025-10-09 | |
Multiply Labs | 2024-09-24 | |
MaxCyte | 2024-05-22 | |
Novartis,Johnson & Johnson | 2024-03-30 | |
Janssen Pharma | 2022-04-21 | |
Noile-Immune Biotech | 2020-05-04 |
Legend Biotech と似ている企業
ペプチド抗原を修飾リポソーム粒子に封入して投与するワクチン、および神経変性疾患のタンパク質凝集体に結合する中枢移行性の低分子化合物を開発する企業。修飾リポソーム技術(SupraAntigen)は、リポソーム表面にアジュバント分子の提示、並びにパルミチン鎖アンカーに連結したAβペプチドなどの標的抗原ペプチドをB-cell peptideとしてリポソーム表面に提示し、リポソーム内に免疫刺激用のT cell peptideを含めることで、標的抗原に対する抗体産生を効率的に誘導する特徴がある。ワクチンとしての利用以外に、動物免疫による抗体作成用の抗原として利用することもできる。タンパク質凝集体に結合する中枢移行性の低分子化合物の探索では、皮質ニューロンの細胞アッセイによって化合物のスクリーニングを行い、Tauやα-synucleinに結合する化合物を特定。共にPETトレーサーとして研究開発を行っている。これまでにp-Tau抗体の品目SemorinemabでGenentechと提携、pTauワクチンでJanssenと提携、Tau PETトレーサーでEli Lillyと提携し、大手製薬企業との提携実績が豊富である。

