Acquired
CAR-T療法やTCR-T療法を開発する企業。遺伝子治療薬を開発するBluebird bio社のスピンオフ企業。Bristol Myers Squibb社と提携し共同開発したBCMA標的CAR-T療法の品目ABECMAが2021年にFDA承認を取得している。後続する免疫細胞療法のパイプラインは様々な技術改善が加えられており、低分子化合物投与によるConditionalな作用技術(DARIC)や、複数の腫瘍抗原を標的とする受容体設計(Dual-/Multiplex-Targeting)、免疫抑制シグナルを活性化シグナルに変換する技術(Reversal of Immunosuppression)や免疫活性化のシグナルを多様化させた改良技術(Co-Stimulation)、TALEN遺伝子編集技術や製造時の効率改善技術などを保有する。2025年にBristol Myers Squibb社と合併している。
Cambridge, Massachusetts, United States
この企業の詳細情報の作成をご希望の方は、お気軽にリクエストください
設立 2021 年 | 推定従業員数 501-1000 名 | 累計調達額 $315M Ave:155.4M Med:22.4M | 提携企業数 9件 Ave:3.3 Med:1 | 論文数 18件 Ave: 13.2 Med: 4 | 特許数 53件 Ave: 13.2 Med: 4 |
テクノロジー
DARIC (Dimerizing Agent Regulated Immunoreceptor Complex)
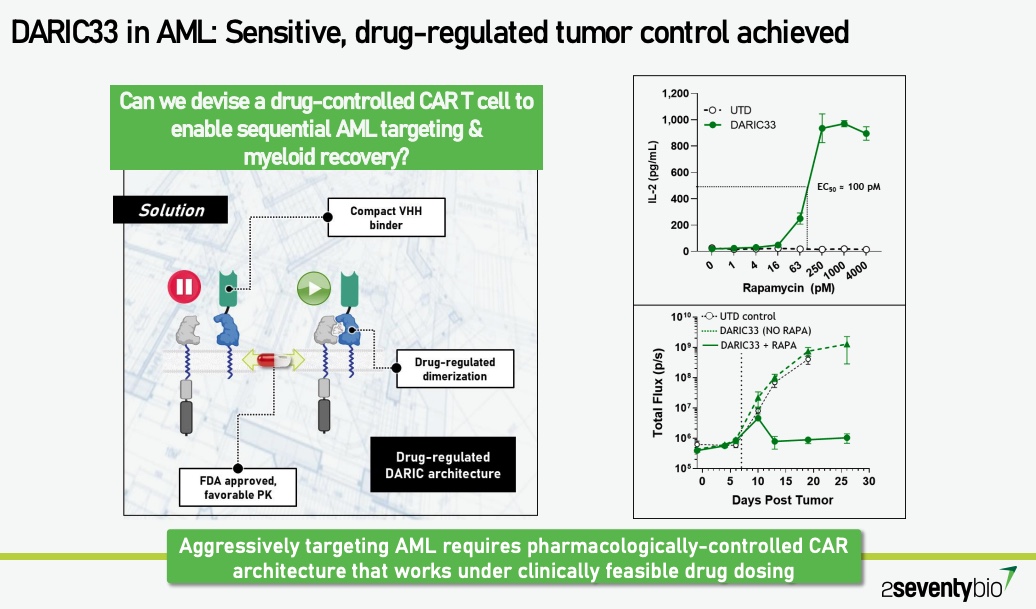
腫瘍抗原を認識するCAR遺伝子の細胞外ドメインと、細胞内の免疫刺激シグナルドメインとを別々のタンパク質に分割してCAR-T細胞に発現させ、低分子化合物の投与によってそれぞれの分割タンパク質が化合物を挟み込む形でヘテロ2量体を形成し、ConditionalにCAR-T細胞を作用させる技術。
CD33を標的とするAMLの品目(SC-DARIC33)で技術が使用されている。2023年9月時点の企業紹介プレゼン資料では、ラパマイシンの投与によって分割タンパク質が2量体化し、化合物を投与したときにのみCAR-T細胞を活性化させるコンセプトが紹介されている。ラパマイシンは免疫抑制状態にならない程度の濃度の投与でCAR-Tの活性化が起こり、非投与(CAR-T不活性)の状態を作ることでT細胞疲弊を防ぎ長期的なCAR-T細胞の生存を維持し、再発時にラパマイシンの投与によって再度活性を示す事ができると説明している(p.27) 。
細胞モデルや非臨床モデルを用いていると思われるデータが紹介されており、ラパマイシン投与条件下でDARIC-33 CAR-TがIL-2を産生し、抗腫瘍効果を示している(p.28)。
Dual-Targeting, Multiplex-Targeting
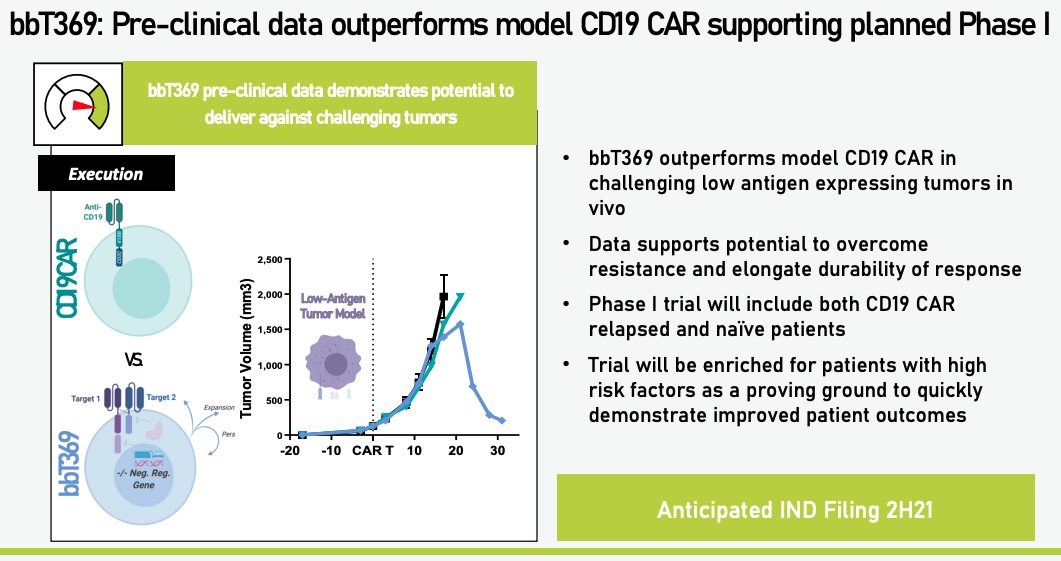
複数の腫瘍抗原を認識したときにCAR-T細胞が活性化するDual CAR-T技術。bbT369、DARIC33 Next-Genの品目で使用されている技術で、bbT369の品目ではCD20とCD79aの2種類の抗原を標的とするCAR遺伝子を発現させ、4-1BBとCD28の共刺激ドメインを分割することで、2種類の抗原が揃ったときにCAR-T細胞が活性化する仕組みが説明されている(p.22)。
加えて、CBLB遺伝子をノックアウトすることでCD28に対する抑制作用を除去し、CAR-T細胞のCell expansionが促進され、長期的な抗腫瘍効果が高まるデータが示されている(p.23)。
DARIC33 Next-Genの技術については、別のプレゼン資料で紹介されている(R&D Deep Diveプレゼン資料p.37)。DARIC技術ではCARを2種類のタンパク質に分割していたが、TCR受容体の構成要素であるCD3 epsilonをヘテロ2量帯の結合ペアとして使用し、ネイティブなTCRシグナルを活性化させてCAR-T活性化の感度を向上させている。
加えて、細胞外ドメインを担うタンパク質については2種類のVHHドメインをタンデムで連結した分子を用いることで、複数種類の腫瘍抗原を認識している。
また、合成プロモーター制御下でsIL-15をコードした遺伝子を導入することで、 TCRシグナルの活性化を受けてsIL-15を発現させるArmored CAR-T技術を紹介している。
これらの改良を全て盛り込んだ品目として、CD33×αCLL1の2種類の抗原を標的とするDARIC Next-Gen CAR-Tの品目27T32が紹介されている(p.43)。
Reversal of Immunosuppression
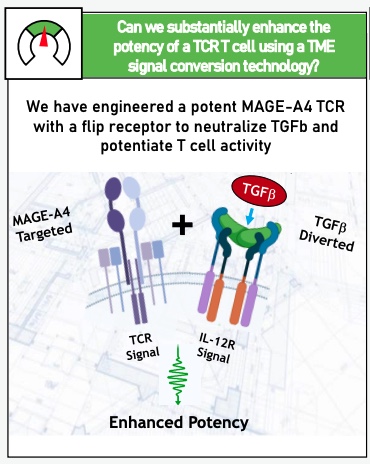
腫瘍微小環境において、投与したT細胞が免疫抑制シグナルを回避する技術。TCR-T療法に使用されている技術で、細胞外にTGF-β受容体ドメインを持ち、細胞内はIL-12Rシグナルを伝達するドメインからなるキメラ受容体を発現させることで、TGF-βの免疫抑制シグナルを免疫活性化シグナルに変換する技術と考えられる。
これによって、TCR受容体の活性化シグナルとかけ合わさって、IFN-γ産生量が増加し抗腫瘍効果が高まるデータを報告している(p.32) 。このキメラ受容体をCAR-T細胞に発現させることも可能だと考えられ、”FLIP receptor”と名付けられた同じ見た目の受容体が紹介されていた(p.31)。
Co-Stimulation
Reversal of Immunosuppressionの応用技術と思われる。詳細不明。
標的、共刺激、サイトカイン受容体のシグナル伝達ドメインをうまく組み合わせることでこれまでと違う強力な抗腫瘍応答を生み出すとの記載がある。
Gene Editing
TALEN由来のDNA結合ドメイン(TALドメイン)をメガヌクレアーゼドメインと融合した遺伝子編集ヌクレアーゼ分子(megaTAL)。
TALドメインは標的配列に応じて設計を行い、加えてメガヌクレアーゼドメイン自体にDNA配列の認識機能があるため、TALとメガヌクレアーゼの両方のDNA配列認識機能をもって切断部位の特異性を高め、off-target効果を抑えることができる (R&D Deep Diveプレゼン資料p.45)。
また、megaTALバリアントの活性・切断配列特異性を評価するスクリーニング系を構築しているため(p.45右図)、より活性や特異性の高いmegaTALバリアントを探索・特定している可能性がある。
CAR-Tでは、bbT369の品目でCBLB遺伝子のノックアウト編集に本技術が使用されている(p.48)。
パイプライン名 | 開発フェーズ | 対象疾患 | 標的分子/作用機序 | モダリティ | パートナー企業 |
|---|---|---|---|---|---|
Abecma (IDE-CEL, bb2121) | 探索 非臨床 P1 P2 P3 申請 上市 | Multiple Myeloma (MM) | BCMA CAR-T | 細胞治療 | |
DARIC33 | 探索 非臨床 P1 P2 P3 申請 上市 | Acute Myeloid Leukaemia (AML) | CD33 CAR-T | 細胞治療 | |
bbT369 | 探索 非臨床 P1 P2 P3 申請 上市 | B-Cell Non Hodgkin Lymphoma (B-Cell NHL) | CD79a, CD20 CAR-T | 細胞治療 | |
DARIC33 NEXT-GEN | 探索 非臨床 P1 P2 P3 申請 上市 | Acute Myeloid Leukaemia (AML) | CD33 CAR-T | 細胞治療 | |
bbT4015 | 探索 非臨床 P1 P2 P3 申請 上市 | Ovarian Cancer | 不明 (CAR-T) | 細胞治療 | |
MEGA-A4 | 探索 非臨床 P1 P2 P3 申請 上市 | Solid Tumors | 不明 | 細胞治療 | |
MULTI-TARGETED CAR T CELL | 探索 非臨床 P1 P2 P3 申請 上市 | Multiple Myeloma (MM) | 不明 (CAR-T) | 細胞治療 | |
MULTIPLE UNDISCLOSAED | 探索 非臨床 P1 P2 P3 申請 上市 | Multiple Myeloma (MM) | 不明 | 不明 |
提携企業
提携企業 | 日付 | プレスリリース |
|---|---|---|
Bristol Myers Squibb | 2025-05-13 | |
Bristol Myers Squibb | 2025-03-25 | |
Novo Nordisk | 2024-06-26 | |
JW Therapeutics | 2023-09-12 | |
JW Therapeutics | 2022-10-27 | |
Bristol Myers Squibb | 2022-01-12 | |
Genevant Sciences | 2022-01-10 | |
Novo Nordisk | 2022-01-06 | |
Bluebird Bio | 2021-11-04 |
2seventy bio と似ている企業
CAR-T療法やγδCAR-T、CAR-NK療法を開発する中国の創薬ベンチャー。BCMAを標的とするCAR-T療法の品目(Carvykti/Ciltacabtagene Autoleucel)がJanssen Pharmaと提携しFDA承認を取得している。抗体スクリーニングを自社で行い、BCMA以外にCD19, CD20, CD22, GPC3, DLL3, Claudin18.2, Guanylyl cyclase-C (GCC)を標的とした品目を血液癌、固形がんを対象に開発する。NHL/ALLを対象に開発されている他家CAR-Tの品目はCD19, CD20, CD22の3種類の抗原を認識する。製造拠点を米国、欧州、中国に保有しグローバルな供給体制を確立。SCLCを対象とするDLL3標的CAR-Tの品目は腫瘍微小環境の免疫抑制シグナルを回避する工夫を施しており、Novartis社に導出を行っている。

