PROTACでは対応が難しい細胞外タンパク質の分解技術を研究する企業。リソソームの細胞分解機構を利用しており、リソソームへのタンパク質輸送シャトル機能を持つマンノース-6-リン酸受容体(M6PR)と結合する化合物を利用して、標的分子をリソソームに輸送するリソソームターゲティングキメラ化合物(LYTAC)を創成する。標的に結合するバインダー分子は抗体やbi-specific抗体、低分子化合物、ペプチドを使用。概念実証の論文では、肝臓特異的なリソソーム関連受容体のASGPRに結合するGalNAcを3量体化し、抗EGFR抗体やインテグリン結合ペプチドと連結したLYTACを報告している。
South San Francisco, California, United States
この企業の詳細情報の作成をご希望の方は、お気軽にリクエストください
設立 2019 年 | 推定従業員数 11-50 名 | 累計調達額 $226.6M Ave:160.7M Med:21M | 提携企業数 3件 Ave:3.6 Med:2 | 論文数 4件 Ave: 12.3 Med: 3 | 特許数 17件 Ave: 19.8 Med: 5 |
テクノロジー
LYTAC (Lysosomal Targeting Chimera)
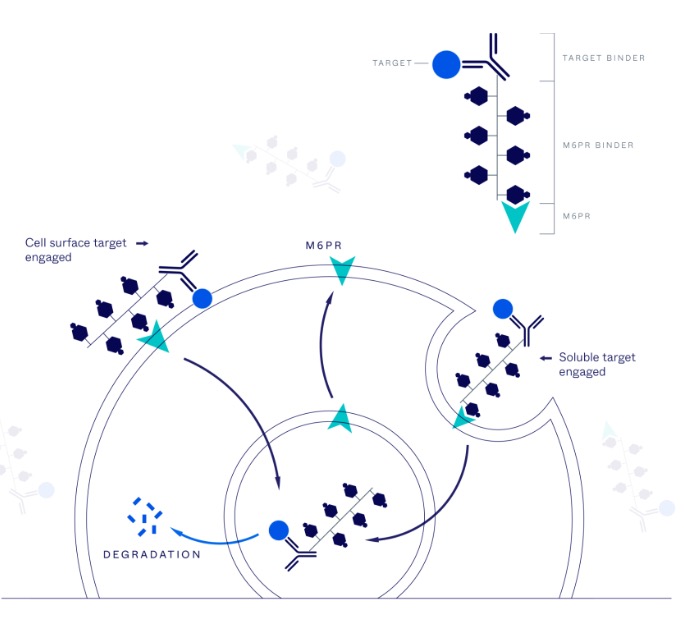
エンドサイトーシスを誘導しリソソームにタンパク質を輸送するシャトル機能を担うmannose-6-phosphate receptor (M6PR)に着目し、M6PRと標的タンパク質とをエンゲージすることで標的タンパク質の分解を誘導するキメラ分子技術。
PROTACと異なり、膜タンパク質、もしくは細胞外のタンパク質を標的とすることができる。
2021年にLYTAC技術を報告した論文では、肝臓特異的なリソソーム関連受容体のASGPRに結合するGalNAcを3量体化し、抗EGFR抗体やインテグリン結合ペプチドと連結したLYTACを報告している。
標的タンパク質に結合する抗体をASGPR結合化合物と連結すればLYTAC化できることから、既存の抗体をdegrader分子に改変できることが興味深い。
M6PR受容体をターゲティングするバインダー分子は最初に報告された2021年の論文ではpoly M6Pを使用していたが、その後の特許ではタンパク質やscFvを使用しており、バインダー分子の改善・最適化を行っていることが伺える。
2022年に申請された特許では、M6PRに対するバインダー分子としてIGF-2タンパク質を使用しており、(Fig.1,2)、IgE抗体を標的とするomalizumabにIGF-2をconjugateしM6PR発現細胞で特異的にomalizumab IGF-2融合分子が取り込まれることを示している(Fig.4。分解誘導活性は評価していない)
2024年の特許では、標的タンパク質とM6PRにそれぞれ結合するarmを持ったbi-specific抗体や、標的タンパク質に対するIgG抗体にM6PR標的scFvをconjugateした抗体分子が示されている(Fig.1)。
CataLYTAC Degrader
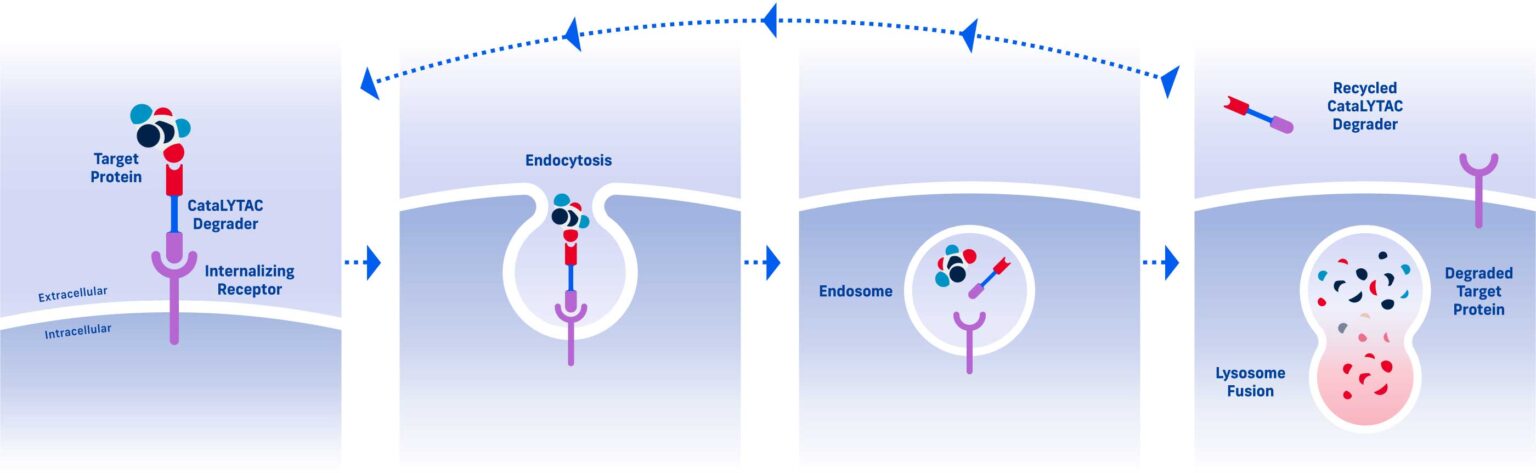
分解を誘導するLYTAC degrader分子自体が分解されずに繰り返し利用されることで、1分子のLYTACが複数の標的分子の分解を誘導することができる技術。
技術に関連する特許が2024年に申請されている。
LYTAC分子自身がLysosomeに移行して分解されることを防ぐため、エンドソームの低pH環境依存的にM6PRやASGPRなどのターゲティング受容体よりもFcRnに親和性高く結合するようにLYTAC分子をFc変異導入などのエンジニアリングによって最適化を行っている。
これにより、LYTAC分子は分解されずリサイクルされる、リサイクリングLYTAC抗体となる(Fig.1B, 項目[0536]〜[0538])。
パイプライン名 | 開発フェーズ | 対象疾患 | 標的分子/作用機序 | モダリティ | パートナー企業 |
|---|---|---|---|---|---|
LCA-0061 | 探索 非臨床 P1 P2 P3 申請 上市 | Allergy | Immunoglobulin E CataLYTAC Degrader | 低分子化合物 | |
LCA-0321 | 探索 非臨床 P1 P2 P3 申請 上市 | Graves' Disease | a-TSHR AAbs LYTAC degrader | 低分子化合物 | |
LCA-0391 | 探索 非臨床 P1 P2 P3 申請 上市 | Graves' Disease | a-MuSK AAbsLYTAC degrader | 低分子化合物 | |
Undisclosed | 探索 非臨床 P1 P2 P3 申請 上市 | Autoimmune disorders | Antigen-specific AAbs LYTAC degrader | 低分子化合物 | |
Undisclosed | 探索 非臨床 P1 P2 P3 申請 上市 | Inflammatory Disorders | Undisclosed CataLYTAC Degrader | 低分子化合物 | |
Multi-target collaboration | 探索 非臨床 P1 P2 P3 申請 上市 | Pain | 不明 | 低分子化合物 | Eli Lilly |
提携企業
提携企業 | 日付 | プレスリリース |
|---|---|---|
Eli Lilly | 2024-05-13 | |
Nona Biosciences | 2023-12-03 | |
Eli Lilly | 2021-08-25 |
Lycia Therapeutics と似ている企業
ペプチド抗原を修飾リポソーム粒子に封入して投与するワクチン、および神経変性疾患のタンパク質凝集体に結合する中枢移行性の低分子化合物を開発する企業。修飾リポソーム技術(SupraAntigen)は、リポソーム表面にアジュバント分子の提示、並びにパルミチン鎖アンカーに連結したAβペプチドなどの標的抗原ペプチドをB-cell peptideとしてリポソーム表面に提示し、リポソーム内に免疫刺激用のT cell peptideを含めることで、標的抗原に対する抗体産生を効率的に誘導する特徴がある。ワクチンとしての利用以外に、動物免疫による抗体作成用の抗原として利用することもできる。タンパク質凝集体に結合する中枢移行性の低分子化合物の探索では、皮質ニューロンの細胞アッセイによって化合物のスクリーニングを行い、Tauやα-synucleinに結合する化合物を特定。共にPETトレーサーとして研究開発を行っている。これまでにp-Tau抗体の品目SemorinemabでGenentechと提携、pTauワクチンでJanssenと提携、Tau PETトレーサーでEli Lillyと提携し、大手製薬企業との提携実績が豊富である。

